Antibioottiresistenssi—evoluution todiste?
Alkuperäisjulkaisu: Creation 39(4):46–48 lokakuu 2017
Julkaistu suomeksi: Luominen–lehti nro 29, s.39–41, 25 toukokuun 2018

Antibioottien keksiminen oli eräs lääketieteen tärkeimmistä edistysaskelista. Se on parantanut merkittävästi ihmiskunnan terveyttä. Ihmisiä tappaneet bakteeritulehdukset, kuten tuberkuloosi ja haavojen tulehdukset, on nyt mahdollista hoitaa, ja tämä on pelastanut miljoonia ihmishenkiä.
Antibioottien tultua käyttöön 1930-luvulla, vuosittaiset kuolemantapaukset esimerkiksi USA:ssa vähenivät käyttöä seuranneiden noin 15 vuoden aikana 220 kuolemalla sataatuhatta ihmistä kohti. Kaikki muut lääketieteelliset teknologiat vähensivät seuraavien 45 vuoden aikana vuosittaisia kuolemia yhteensä vain noin 20 kuolemalla sataatuhatta ihmistä kohti.1
Vastustuskyky antibiooteille uhkaa kuitenkin tätä suotuisaa kehitystä. Monille tai kaikille antibiooteille vastustuskykyisten bakteerien aiheuttamat tulehdukset lisääntyvät maailmanlaajuisesti. Lisäksi yhä harvemmat lääkeyritykset kehittävät uusia antibiootteja. Vuonna 1990 antibiootteja kehittäviä lääkeyrityksiä oli vielä 18, mutta vuonna 2011 alalla toimi enää neljä yritystä.2 Tämä johtuu siitä, että vastustuskyky uudelle antibiootille tulee nopeasti esiin sen markkinoille tulon jälkeen, ja uusien antibioottien kehittäminen on hyvin kallista. Kun vuonna 2015 ilmoitettiin uuden antibioottien ryhmän keksimisestä, tämä tapahtui ensimmäistä kertaa sitten vuoden 1987.3
Koulujen ja yliopistojen biologian oppikirjat väittävät yleensä, että vastustuskyky antibiooteille olisi esimerkki ‘toimivasta evoluutiosta’ ja tämä todistaisi, että mikrobit voisivat muuttua mikrobiologeiksi miljardien vuosien kuluessa. Ilmiön taustalla olevien biokemiallisten mekanismien tutkiminen osoittaa kuitenkin, että vastustuskyvyn ilmaantuminen ei tue väitetyn kaltaisia suuren mittaluokan evoluutiomuutoksia. Havaitut muutokset tukevat luomisopin mukaista näkemystä eliömaailmasta, missä tapahtuvat luonnolliset muutokset ovat rajallisia, eivätkä voi johtaa eliöiden muuttumiseen yhdestä luodusta lajityypistä toiseksi.
Vastustuskyvyn mekanismit
Tutkijat ovat löytäneet vastustuskyvyn ilmaantumiselle kolme pääasiallista tapaa:
- Antibiootin vaikutuskohteen muuttaminen tai suojaaminen
- Lääkkeen kohteeseen pääsyn rajoittaminen
- Antibiootin tekeminen tehottomaksi (inaktivointi).
1. Antibiootin vaikutuskohteen muuttaminen tai suojaaminen
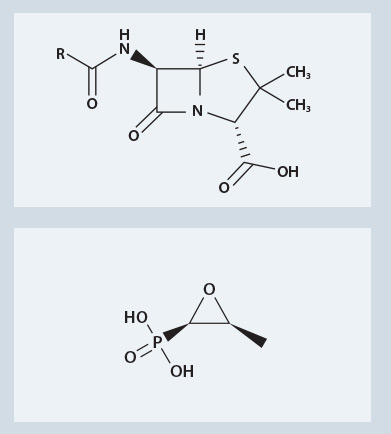
Kolistiini (joka tunnetaan myös nimellä polymyksiini E) tarjoaa esimerkin. Ihmisen kehossa kolistiini on positiivisesti varautunut molekyyli, joka kiinnittyy negatiivisesti varautuneisiin molekyyleihin (lipopolysakkarideihin LPS), joita on tiettyjen (gram-negatiivisten bakteerien) ulommassa solukalvossa. Tämä kiinnittyminen on ensimmäinen ja keskeinen vaihe bakteereja tappavassa tapahtumassa.
Jossakin yksittäisessä bakteerissa mutaatiot voivat estää LPS:n tuotannon. Tämä estää kolistiinin kiinnittymisen—ja bakteeri selviää hengissä.4
On monimutkaisempiakin mekanismeja, jotka estävät antibiootin kiinnittymisen. Positiivisesti varautuneet magnesium-ionit, jotka sitoutuvat negatiivisesti varautuneisiin LPS-molekyyleihin, vakauttavat normaalisti tämän tyyppisten bakteerien solukalvon. Kun magnesiumpitoisuus on matala, bakteereilla on järjestelmä, jolla ne peittävät negatiiviset varaukset solukalvon säilyttämiseksi vakaana. Solulla on säätelyjärjestelmiä varausten peittämisen hallintaan. Niitä kytketään päälle vain tarvittaessa. Mutaatio voi vaurioittaa säätelyjärjestelmää, mikä voi johtaa peittämisjärjestelmän jatkuvaan toimintaan. Solu ei voi silloin kääntää sitä pois päältä. Negatiivisten varausten määrän väheneminen johtaa silloin siihen, ettei antibiootti voi nytkään kiinnittyä soluun ja tappaa sitä. Tässä tapauksessa mutatoitunut solu hukkaa resurssejaan tilanteessa, jossa järjestelmää ei tarvita eli bakteeri selviytyy huonommin silloin, kun antibioottia ei ole ympäristössä [tappamassa sen kilpailijoita].
Katsotaan asiaa miten päin tahansa, mutaatiot rikkovat olemassa olevia toimintoja sen sijaan, että ne kehittäisivät jonkin uuden mekanismin, johon sisältyisi uusien entsyymien ja proteiinien toiminta.
2. Lääkkeen kohteeseen pääsyn rajoittaminen
Monien antibioottien on päästävä sisälle bakteeriin, jotta ne voivat tappaa sen. Esimerkkinä tästä on fosfomysiini, joka tappaa bakteerit estämällä niitä valmistamasta erästä soluseinämän välttämätöntä ainesosaa. Bakteerien soluseinämässä on erilaisia ‘pumppuja’, jotka kuljettavat ravinteita soluun. Vaikka pumppujen siirtäjämolekyylit ovat hyvin valikoivia siinä, mitä ne kuljettavat, fosfomysiini muistuttaa rakenteeltaan niiden kuljettamia tavallisia ravinteita, joten se pääsee siirtymään solun sisälle.
Mutaatiot niissä geeneissä, jotka määräävät, miten solu valmistaa näiden pumppujen siirtäjämolekyylit, tai säätelygeeneissä, jotka lisäävät niiden tuotantoa, voivat aiheuttaa sen, että pumppuja ei valmistu lainkaan tai ne ovat tehottomampia. Tästä seuraa, että fosfomysiiniä ei pääse lainkaan tai vain hyvin niukasti solun sisälle. Nämä solut ovat fosfomysiinille vastustuskykyisiä.
Jälleen kerran mutaatiot tuhoavat solun normaalin toiminnan eivätkä luo uusia geenejä, uusia proteiineja tai entsyymejä. Tämä on kaukana siitä ajatuksesta, että vastustuskykyinen solu olisi ‘uusi paranneltu malli’, sillä nämä solut eivät myöskään kykene kuljettamaan tavallisia ravinteita normaaleja määriä, koska pumput ovat nyt vahingoittuneita tai puuttuvat. Niinpä antibiootin poissa ollessa sille herkät bakteerit syrjäyttävät vastustuskykyiset bakteerit, ja lopulta vastustuskykyiset yksilöt muodostavat vain pienen osan kokonaisbakteerikannasta.
Käänteiset pumput
Monilla bakteerilajeilla on pumppuja, jotka työntävät erilaisia aineita, myös myrkyllisiä, ulos solusta. Niitä kutsutaan ‘ulosvirtauspumpuiksi’. Nämä voivat pumpata myös antibiootteja ulos solusta ja estävät näin antibioottia tappamasta sitä. Ulosvirtauspumppujen valmistukseen liittyvien geenien säätely on monimutkaista, mutta pumppujen lukumäärää rajoittavien säätelijöiden mutaatiot voivat johtaa monien lisäpumppujen tuottamiseen, jolloin solusta tulee vastustuskykyinen antibiootille. Tämän tyyppinen vastustuskyky on erityisen tärkeää fluorokinolonien luokkaan kuuluville antibiooteille.5 Voidaan todeta, että tässäkin viallinen säätelyjärjestelmä tuhlaa solun voimavaroja, kun se valmistaa ylimääräisiä pumppuja silloin, kun niitä ei tarvita. Tämän mutaation sisältävät solut säilyvät huonommin elossa silloin, kun antibioottia ei ole ympäristössä.
Kaikissa näissä tapauksissa mutaatiot ‘rikkovat’ geenejä, jotka valmistavat pumppuja tai ohjaavat niiden tuotantoa. Tämä ei tue ajatusta mutaatioista, jotka loisivat uusia evoluution tarvitsemia geenejä, jotta bakteereista voisi kehittyä bakteriologeja.

3. Antibiootin tekeminen tehottomaksi (inaktivointi)
Bakteerin valmistamat entsyymit voivat hajottaa antibiootin siinä aineenvaihduntatapahtumassa, jota ne suorittavat. Esimerkiksi beeta-laktamaaseiksi kutsutut entsyymit voivat hajottaa penisilliinit. Voisi näyttää siltä, että bakteeri, joka on kohdannut antibiootin ja sen jälkeen hankkii tällaisen kyvyn, olisi merkittävä esimerkki evoluutiosta—uusi entsyymi ja uusi geeni. Antibiootteja hajottavan entsyymin valmistuskoneiston ei kuitenkaan ole koskaan havaittu syntyvän mutaation avulla. Miten se sitten tapahtui?
Geeninsiirto
Nykyään tiedetään, että bakteerisolu voi saada antibiootin hajottamiskyvyn toiselta bakteerilta, joka on jo vastustuskykyinen.
Tällaisen vastustuskyvyn geenit voivat sijaita pienissä plasmideiksi kutsutuissa DNA-silmukoissa, jotka ovat bakteerin varsinaisen rengasmaisen kromosomin ulkopuolella. Nämä plasmidit voivat siirtyä bakteerista toiseen ja jopa lajista toiseen.6 Bakteeri, jolla on vastustuskyvyn antava plasmidi, siirtää plasmidin herkkään bakteeriin eräänlaisen siirtoputken (pilus) välityksellä.7 Vastustuskykyinen bakteeri kopioi plasmidin ja ‘lahjoittaa’ kopion antibiootille herkälle yksilölle (katso kaaviota yllä).
Monet plasmidit sisältävät useita vastustuskyvyn antavia geenejä monille eri tyyppisille antibiooteille.
Tämän tyyppiseen vastustuskykyyn ei tässäkään tapauksessa sisälly minkäänlaista uusien geenien syntymistä, vaan olemassa olevat geenit siirtyvät vastustuskykyiseltä bakteerilta herkälle bakteerille.8
Valvontajärjestelmien rikkoutuminen
Vastustuskyky penisilliinille tarjoaa perinteisen esimerkin. Eräät bakteerit tuottavat pieniä määriä penisillinaasia hajottaakseen niiden elinympäristössä luonnollisesti esiintyvät pienet penisilliinimäärät, mutta eivät tuota sitä riittävästi selviytyäkseen potilaille annetusta määrästä. Penisillinaasin valmistusta rajoittavassa järjestelmässä tapahtuva mutaatio voi johtaa siihen, että bakteeri tuottaa penisillinaasia paljon enemmän, ja bakteerista tulee vastustuskykyinen. Mutta samalla tavoin kuin joissakin aikaisemmin mainituissa tapauksissa nämä vastustuskykyiset bakteerit, jotka eivät enää pysty hallitsemaan penisillinaasin tuotantoaan, jäävät luonnossa alakynteen verrattuna bakteereihin, jotka eivät tuhlaa niukkoja voimavarojaan penisillinaasin liikatuottoon.
Luonnonvalinta?
Kaikissa niissä tapauksissa, joissa antibiootteja on runsaasti ympäristössä, luonnonvalinta suosii vastustuskykyisiä kantoja. Vaikka luonnonvalinta selittää vastustuskyvyn säilymisen tällaisessa tilanteessa, se ei kuitenkaan selitä sen syntymistä. Vastustuskyky johtuu olemassa olevan järjestelmän muokkaamisesta (yleensä sen rikkomisesta) tai vastustuskyvyn antavien geenien siirtämisestä bakteerilta toiselle. Silloin, kun mutaatio on rikkonut jotakin, luonnonvalinta pyrkii luonnon olosuhteissa poistamaan samat vastustuskykyiset kannat, joita se suosii antibioottien kyllästämässä ympäristössä.
Johtopäätös
Vastustuskyvystä tehdyt tutkimukset ovat paljastaneet mutaatioista ja luonnonvalinnasta joitakin hyviä esimerkkejä, joissa bakteeria on autettu sopeutumaan antibioottien läsnäoloon. Yksikään havainto ei kuitenkaan tue väitettä, jonka mukaan satunnaiset muutokset (mutaatiot) olemassa olevien geenien DNA:ssa voisivat tuottaa monia tuhansia uusia geenejä ja geeniverkostoja, joita tarvitaan muuntamaan mikrobit mikrobiologeiksi, mangoiksi ja mursuiksi. Tutkimushavainnot alleviivaavat sen sijaan mutaatioiden rajallista kykyä tuottaa ‘ylöspäin suuntautuvaa’ evoluutiota.
Lähdeluettelo ja kommentit
- Spellberg, B., The antibacterial pipeline: why it is drying up, and what must be done about it, In: Antibiotic Resistance: Implications for Global Health and Novel Intervention Strategies: Workshop Summary, National Academies Press, p. 327, 2011. Palaa tekstiin.
- Cooper, M.A. and Shlaes, D., Fix the antibiotics pipeline, Nature 472(7341):32, 2011 | doi:10.1038/472032a. Palaa tekstiin.
- Ling, L.L. et al., A new antibiotic kills pathogens without detectable resistance, [suomeksi: Uusi antibiootti tappaa taudinaiheuttajia ilman havaittavaa resistenssiä] Nature 517(7535):455–459, 2015 | doi:10.1038/nature14098; the antibiotic is called teixobactin. Palaa tekstiin.
- Moffatt, J.H. et al., Colistin resistance in Acinetobacter baumannii is mediated by complete loss of lipopolysaccharide production, [suomeksi: Acinetobacter baumanniin kolistiiniresistenssi johtuu lipopolysakkaridituotannon täydellisestä menetyksestä.] Antimicrob. Agents Chemother. 54(12):4971–7, 2010 | doi: 10.1128/ AAC.00834-10. Palaa tekstiin.
- Blair, J.M.A., Richmond, G.E., and Piddock, L.J.V., Multidrug efflux pumps in Gram-negative bacteria and their role in antibiotic resistance (review), [suomeksi: Monilääkkeiden ulosvirtauspumput gramnegatiivisissa bakteereissa ja niiden rooli antibioottiresistenssissä (arvostelu)] Future Microbiology 9(10):1165–1177, 2014 | doi:10.2217/fmb.14.66. Palaa tekstiin.
- On muitakin tapoja, joilla vastustuskyvyn geenejä voidaan siirtää, kuten bakteriofagit (virus, joka tunkeutuu bakteereihin), transposonit ja ‘paljas DNA’. Palaa tekstiin.
- Tätä kutsutaan ‘konjugaatioksi’. Palaa tekstiin.
- Evolutionistit olettavat, että näiden geenien (esimerkiksi penisilliiniä tuhoavan beeta-laktamaasi-entsyymin valmistamiseksi) on täytynyt alun perin syntyä mutaatioiden avulla, mutta tämä on uskomus, joka ei perustu havaintoihin. Palaa tekstiin.

Readers’ comments
Comments are automatically closed 14 days after publication.